Рибосомы у вирусов оспы
Вирусы оспы. Виды вирусов оспы. Строение вирусов оспы.
Вирусы оспы (ВО) — самые крупные вирусы, содержащие ДНК, молекулярная масса которой больше, чем у любого другого вируса животных. Они широко распространены в природе, вызывают заболевания позвоночных и беспозвоночных с летальным исходом или в виде легко протекающей продолжительной инфекции с образованием доброкачественных опухолей. ВО передаются членистоногими при прямом контакте, аэрозольно или механически. ВО обычно имеют узкий круг хозяев, хотя некоторые из них представляют исключения, в том числе вирусы вакцины и оспы птиц. Вирусы оспы позвоночных включают восемь родов (орто-, пара-, ави-, капри-, лепори-, суи-, моллюсци- и ятапоксвирусы).
Разделение вирусов оспы позвоночных на роды проведено с учетом массы и структуры генома, размера и формы вириона, способности к генетической рекомбинации, антигенной связи и спектра патогенности.
Ортопоксвирусы. Типичный представитель — вирус осповакцины (ВОВ). Спектр естественных хозяев узкий, обычно ограничен одним видом животных: вирусы агглютинируют эритроциты цыплят; варьируют по вирулентности для естественных хозяев и лабораторных животных. Другие виды: вирусы оспы буйволов, верблюдов, крупного рогатого скота, мышей, обезьян и вирус натуральной оспы.
Парапоксвирусы. Типичный представитель — вирус контагиозного пустулёзного дерматита (эктимы) овец и коз (вирус орф). Представители рода серологически связаны между собой, но отличаются от представителей других родов; гемагглютинин не образуют. Другие виды: вирусы пустулёзного стоматита крупного рогатого скота, контагиозной эктимы серн и сыпи доярок.
Авипоксвирусы. Естественные хозяева — птицы; типичный представитель — вирус оспы кур. Члены рода серологически связаны между собой. Другие виды: вирусы оспы канареек, голубей, перепелов, воробьев, скворцов, индеек и оспы Юнко. Передаются членистоногими.
Каприпоксвирусы. Естественные хозяева — парнокопытные; типичный представитель — ВО мелких жвачных (овец и коз). В данный род входит также вирус кожной бугорчатки крупного рогатого скота.
Лепорипоксвирусы. Типичный представитель — вирус миксомы кроликов. Передается механически членистоногими. Другие виды: вирусы фибромы зайцев, кроликов (вирус Шоупа) и белок. Вирус злокачественной фибромы кроликов — летальный туморогенный поксвирус, возникший, по-видимому, вследствие рекомбинации между вирусами фибромы и миксомы кроликов.
Суипоксвирусы. Типичный представитель — вирус оспы свиней. В инфицированных клетках образуются несколько типов цитоплазматических включений и наблюдается вакуолизация ядра. Другие члены рода не определены.
Моллюсципоксвирусы. Типичный представитель — вирус контагиозного моллюска. Возможные члены рода — вирусы однокопытных и обезьян.
Ятапоксвирусы включают вирус опухолей обезьян Яба и вирус оспы Тана.
Вирусы оспы — наиболее крупные из всех вирусов животных. Под электронным микроскопом они выглядят как большие овальные (кирпичеобразные) частицы размером около 250-350×200-270 нм.
Орто-, ави-, лепорипоксвирусы более вытянуты, а вирус оспы свиней шире, чем другие ВО. Парапоксвирусы имеют овальную (коконообразную) форму и размер 260×160 нм.
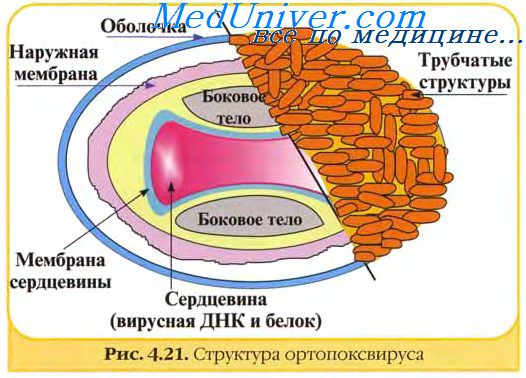
В структуре вирусов оспы различают три основных компонента: двояковогнутую сердцевину, овальные боковые тела и оболочку вириона. Сердцевину вириона составляют ДНК и связанные с нею белки. Сердцевина окружена гладкой мембраной (толщиной около 5 нм), снаружи покрытой слоем вертикально уложенных и плотно прилегающих друг к другу цилиндрических субъединиц (5×10 нм). Вогнутость сердцевины с обеих сторон занята овальными образованиями (неизвестной природы), называемыми боковыми телами. Они как бы сдавливают сердцевину, придавая ей форму двояковогнутого диска, имеющего на разрезе вид гантели.
Вирионы заключены в липопротеиновую супероболочку, которая имеет толщину 20—30 нм и содержит липиды клетки и вирусспецифические белки.
Вирионы большинства вирусов оспы окружены слоем беспорядочно расположенных трубчатых структур, придающих им характерный вид. Эти структуры состоят из сферических субъединиц диаметром около 5 нм. Субъединицы построены из молекул протеина или гликопротеина. В состав ворсинок длиной 20 нм покрывающих поверхность вируса осповакцины (ВОВ), входит белок с молекулярной массой 58 кД, относящийся к главным полипептидам вириона. Поверхность парапоксвирусов покрыта длинными нитеподобными трубочками, уложенными крест-накрест, напоминающими клубок пряжи.
Вирус осповакцины содержит белки, липиды и ДНК, которые соответственно составляют 90, 5 и 3,2% массы вириона (5х10~15 г). В вирусе оспы птиц около 1/3 массы составляют липиды.
Вирион образуется включением ДНК внутрь незрелых вирусоподобных частиц, которые затем созревают, покрываясь дополнительно наружными оболочками. Репликация и сборка вирионов происходят в разных местах цитоплазмы (в виропластах или вирусных фабриках), и вирионы освобождаются почкованием или при лизисе клеток.
Вирионы, освободившиеся из клетки почкованием до ее разрушения, покрыты оболочкой, которая содержит клеточные липиды и несколько вирусспецифических белков.
— Также рекомендуем «Геном вирусов оспы. Антигены вирусов оспы.»
Оглавление темы «Частная вирусология.»:
1. ДНК-вакцины. Свойства и методы получения днк-вакцин.
2. Синтетические пептидные вакцины. Свойства синтетических пептидных вакцин.
3. Вирусы оспы. Виды вирусов оспы. Строение вирусов оспы.
4. Геном вирусов оспы. Антигены вирусов оспы.
5. Оспа овец. Оспа птиц. Особенности оспы овец и птиц.
6. Контагиозный пустулёзный дерматит. Эктима. Миксоматоз.
7. Асфаровирусы. Признаки и свойства асфаровирусов.
8. Иридовирусы. Герпесвирусы. Семейство герпесвирусов.
9. Эпидемиология герпесвирусов. Строение герпесвирусов.
10. Антигены вируса герпеса. Протеины герпесвирусов.
Источник

Интерферон и рибосомы отнимают у вирусов жизнь
— Каким же образом действует интерферон на вирус? Может ли он соединяться с вирусом и нейтрализовать его, как это делают антитела?
— Нет, инферферон с вирусом не соединяется, и в этом одно из его решающих отличий от антител.
— Но, может быть, интерферон не дает вирусу адсорбироваться на клеточной оболочке, или как-то мешает ему проникнуть внутрь клетки, или, действуя на вирусную нуклеиновую кислоту, инактивирует ее?
— Вот здесь вы несколько ближе к истине, Люди часто стараются найти уже известные аналогии для объяснения нового и непонятного. Так произошло и с интерфероном, действие которого на вирусы совершенно необычное.
Многие ученые в разных странах мира обнаружили, что интерферон наделен необычайно широким «спектром» противовирусной активности: он подавляет размножение большинства известных вирусов. Препятствует размножению вируса оспы в коже, вируса гриппа в легких, вируса энцефалита в мозгу, вируса лейкоза в костном мозге или в лейкоцитах крови.
Механизм такого бесконечного универсализма должен быть единым, направленным на какой-то общий этап размножения всех этих паразитов. В этом огромное преимущество интерферона перед антителами, которые соединяются, а затем нейтрализуют строго специфически лишь тот вирус, который вызвал их образование (например, антитела против вируса гриппа типа А не действуют даже на вирус гриппа типа В).

Подавление…
Уже первые поиски установили, что непосредственного воздействия на вирус интерферон не оказывает. Действительно, пробовали соединить в пробирке вирусную суспензию с концентрированными препаратами интерферона, а затем заразить этой смесью животное. И убедились, что инфекционный процесс развивается с такой же интенсивностью, как и при использовании вируса без интерферона.
Расшифровали механизм действия интерферона совсем недавно. И сделали это американский вирусолог С. Барон и наши советские ученые, москвичи Ф. Ершов и В. Жданов в Институте вирусологии имени Д. Ивановского. Они доказали, что весь процесс защиты организма от внедрившегося вируса происходит внутри еще не зараженных клеток, а в 1975 году группа ученых Йельского университета (США) установила, что в ядрах клеток человека, в хромосоме № 21, находится специальная группа генов (специфический участок ДНК, с которым соединяется молекула интерферона, как только она проникает в клетку), отвечающая за этот процесс.
Небольшая молекула интерферона способна свободно проходить через клеточные оболочки и, проникая в цитоплазму, воздействовать на синтетический аппарат клетки так, что он становится непригодным для размножения вирусов. Этот механизм коренным образом отличается от действия антител, которые для выполнения своей функции должны обязательно соединиться с вирусами, находящимися вне клетки. Только таким путем антитела препятствуют переходу вируса от зараженной клетки к здоровой.
К сожалению, процессы, происходящие на уровне таких мелких молекул, какой является интерферон, нельзя увидеть. Но тончайшие методы современной вирусологии и генетики позволяют косвенно проследить за ходом этих процессов.
В. Жданов, Ф. Ершов и их сотрудники установили, что интерферон как бы пробуждает от спячки группу генов, отвечающих за синтез особых информационных РНК, с помощью которых клетка быстро строит антивирусный белок. Дальше события разворачиваются совершенно необычным образом. Вновь синтезированный антивирусный белок используется клеткой не для нейтрализации самого вируса, а для того, чтобы нарушить так хитро налаженный механизм печатания копий вирусных РНК и сделать невозможным воспроизводство вирусного потомства. Все синтетические процессы, необходимые для нормального функционирования самой клетки, сохраняются.
Каждая молекула антивирусного белка присоединяется к одной из рибосом, слегка изменяя этим ее конфигурацию. Такие рибосомы по-прежнему сохраняют способность соединяться под влиянием информационных РНК в полисомные комплексы и строить новые клеточные белки. Однако если полисома сформируется под воздействием вирусной информационной РНК, то дальнейшей передачи информации не будет и синтеза вирусных белков не произойдет.
Некоторые вирусологи считают, что молекула интерферона или даже отдельные ее фрагменты могут соединяться с рибосомами и делать их непригодными для передачи вирусной информации и синтеза компонентов вирусной частицы. Так или иначе, но после контакта с молекулой интерферона каждая клетка превращается в своеобразную ловушку, куда вирус легко попадает и где он находит свою могилу, не выполнив главной задачи паразита — произвести потомство.
Многие ученые говорили о преимущественной защитной роли интерферона при таких кратковременных и остротекущих инфекциях, как грипп. В Научно-исследовательском институте эпидемиологии и микробиологии имени Л. Пастера обследовали большое число сывороток крови людей, заболевших гриппом и лечившихся в больнице имени С. Боткина в Ленинграде. Оказалось, что чем больше интерферона образовывалось в первые дни болезни, тем легче протекал грипп и тем быстрее поправлялся больной. У некоторых людей интерферон вообще препятствовал развитию болезни, хотя скрытая инфекция была и это подтверждалось образованием антител.
Полезное влияние интерферона зависит от степени болезнетворности, зловредности вируса для организма, а также от общего состояния здоровья человека. Защитный эффект интерферона снижается, если возбудитель вирусной инфекции чрезмерно разрушителен, токсичен, а человек ослаблен переутомлением, нервными переживаниями, хроническими заболеваниями сердца, печени, легких.
Когда система интерферона не срабатывала, грипп становился фатальным для больного. Именно это доказал известный английский ученый Д. Тиррелл, обследуя большое число людей, для которых грипп стал причиной смерти. Все они погибли в первые дни заболевания гриппом. Ни у одного из этих людей не удалось обнаружить интерферон ни в легких, ни в крови.
И наоборот, можно считать, что благополучный исход вирусной инфекции является результатом активной оборонительной деятельности зараженных клеток, вырабатывающих интерферон, который нарушает синтез новых вирусных частиц и ликвидирует опасность появления и распространения по организму новых генераций вируса.
Ученые не только доказали, что одним из факторов, определяющих сопротивляемость организма вирусной инфекции, служит его способность вырабатывать интерферон, но и что у разных людей она неодинакова. Большую роль играют врожденные особенности организма. Около трети населения обладают характерными наследственными чертами, вследствие которых их организм плохо производит интерферон. Зависит эта способность и от возраста: интерферон слабее вырабатывается у детей до двухлетнего возраста, а также у пожилых людей старше 60-65 лет.

Формирование интерферона идет по-разному в зависимости от внешних условий
Формирование интерферона идет по-разному в зависимости от внешних условий, например, погоды, температуры воздуха, времени года. Зимой или осенью организм медленнее производит интерферон и в меньших количествах, чем в теплое время. Поэтому летом люди гораздо реже страдают от гриппа и других заболеваний верхнего дыхательного тракта.
Таким образом, фронт борьбы с вирусами пролегает внутри живых клеток. Очень сложен путь его познания и долог. Исследователи находятся сейчас лишь в самом его начале. Однако новые факты, которыми человечество овладело совсем недавно, помогли разгадать, пожалуй, самую сложную загадку — универсальный механизм, с помощью которого природа помогла всем живущим на земле существам одерживать победу над вирусами.
Источник
Сложность статьи
Вирус (от лат. virus — яд) — простейшая форма жизни, микроскопическая частица, представляющая собой молекулы нуклеиновых кислот (ДНК или РНК), заключенные в белковую оболочку (капсид) и способные инфицировать живые организмы.
Вирусы, за редким исключением, содержат только один тип нуклеиновой кислоты: либо ДНК, либо РНК (некоторые, например мимивирусы, имеют оба типа молекул).
Вирусы являются облигатными паразитами, так как не способны размножаться вне клетки. Вне клетки вирусные частицы ведут себя как химические вещества.
В настоящее время известны вирусы, размножающиеся в клетках растений, животных, грибов и бактерий (последних обычно называют бактериофагами). Обнаружены также вирусы, поражающие другие вирусы (вирусы-сателлиты).

Рис. 1 Бактериофаг
Впервые существование вируса (как нового типа возбудителя болезней) доказал в 1892 г. русский ученый Д. И. Ивановский. После многолетних исследований заболеваний растений табака в работе, датированной 1892 г., Д. И. Ивановский приходит к выводу, что табачная мозаика вызывается «бактериями, проходящими через фильтр Шамберлана, которые, однако, не способны расти на искусственных субстратах».
Пять лет спустя, при изучении заболеваний крупного рогатого скота, а именно ящура, был выделен аналогичный фильтрующийся микроорганизм. А в 1898 г., при воспроизведении опытов Д. Ивановского голландским ботаником М. Бейеринком, он назвал такие микроорганизмы «фильтрующимися вирусами». В сокращенном виде это название и стало обозначать данную группу микроорганизмов.
В 1901 г. было обнаружено первое вирусное заболевание человека — желтая лихорадка. Это открытие было сделано американским военным хирургом У. Ридом и его коллегами.
В 1911 г. Фрэнсис Раус доказал вирусную природу рака — саркомы Рауса (лишь в 1966 г., спустя 55 лет, ему была вручена за это открытие Нобелевская премия по физиологии и медицине).
В последующие годы изучение вирусов сыграло важнейшую роль в развитии эпидемиологии, иммунологии, молекулярной генетики и других разделов биологии. Так, эксперимент Херши и Чейза стал решающим доказательством роли ДНК в передаче наследственных свойств. В разные годы еще как минимум шесть Нобелевских премий по физиологии и медицине и три Нобелевских премии по химии были вручены за исследования, непосредственно связанные с изучением вирусов.
В 2002 г. в Нью-Йоркском университете был создан первый синтетический вирус (вирус полиомиелита).
Строение вирусов
Просто организованные вирусы состоят из нуклеиновой кислоты и нескольких белков, образующих вокруг нее оболочку — капсид. Примеров таких вирусов является вирус табачной мозаики. Его капсид содержит один вид белка с небольшой молекулярной массой.

Рис. 2 Вирус табачной мозаики
Сложно организованные вирусы имеют дополнительную оболочку — белковую или липопротеиновую; иногда в наружных оболочках сложных вирусов помимо белков содержатся углеводы. Примером сложно организованных вирусов служат возбудители гриппа и герпеса. Их наружная оболочка — это фрагмент ядерной или цитоплазматической мембраны клетки-хозяина, из которой вирус выходит во внеклеточную среду.

Рис. 3 Вирус гриппа
Распространение вирусов на Земле
Вирусы являются одной из самых распространенных форм существования органической материи на планете по численности: воды мирового океана содержат колоссальное количество бактериофагов (около 250 миллионов частиц на миллилитр воды), их общая численность в океане — около 4×$10^{30}$, а численность вирусов (бактериофагов) в донных отложениях океана практически не зависит от глубины и всюду очень высока. В океане обитают сотни тысяч видов (штаммов) вирусов, подавляющее большинство которых не описаны и тем более не изучены. Вирусы играют важную роль в регуляции численности популяций некоторых видов живых организмов (например, вирус дикования раз в несколько лет сокращает численность песцов в несколько раз).
Генетические связи и происхождение вирусов
Вирусы имеют генетические связи с представителями флоры и фауны Земли. Согласно последним исследованиям, геном человека более чем на 32 % состоит из информации, кодируемой вирусподобными элементами и транспозонами. С помощью вирусов может происходить так называемый горизонтальный перенос генов (ксенология), то есть передача генетической информации не от непосредственных родителей к своему потомству, а между двумя неродственными (или даже относящимися к разным видам) особями. Так, в геноме высших приматов существует белок синцитин, который, как считается, был привнесен ретровирусом. Иногда вирусы образуют с животными симбиоз. Так, например, яд некоторых паразитических ос содержит структуры, называемые поли-ДНК-вирусами (Polydnavirus, PDV), имеющие вирусное происхождение.
Вирусы — сборная группа, не имеющая общего предка. В настоящее время существует несколько гипотез, объясняющих происхождение вирусов.
Считается, что крупные ДНК-содержащие вирусы происходят от более сложных (и, возможно, клеточных, таких как современные микоплазмы и риккетсии), внутриклеточных паразитов, утративших значительную часть своего генома. И действительно, некоторые крупные ДНК-содержащие вирусы (мимивирус, вирус оспы) кодируют функционально избыточные, на первый взгляд, ферменты, по-видимому, оставшиеся им в наследство от более сложных форм существования. Следует также отметить, что некоторые вирусные белки не обнаруживают никакой гомологии с белками бактерий, архей и эукариот, что свидетельствует о сравнительно давнем обособлении этой группы.
ДНК-содержащие бактериофаги и некоторые ДНК-содержащие вирусы эукариот, возможно, происходят от мобильных элементов — участков ДНК, способных к самостоятельной репликации в клетке.
Происхождение некоторых РНК-содержащих вирусов связывают с вироидами. Вироиды представляют собой высокоструктурированные кольцевые фрагменты РНК, реплицируемые клеточной РНК-полимеразой. Считается, что вироиды представляют собой «сбежавшие интроны» — вырезанные в ходе сплайсинга незначащие участки мРНК, которые случайно приобрели способность к репликации. Белков вироиды не кодируют. Считается, что приобретение вироидами кодирующих участков (открытой рамки считывания) и привело к появлению первых РНК-содержащих вирусов. И действительно, известны примеры вирусов, содержащих выраженные вироидподобные участки (вирус гепатита Дельта).
Вирусные частицы (вирионы) представляют собой белковую капсулу — капсид, содержащую геном вируса, представленный одной или несколькими молекулами ДНК или РНК. Капсид построен из капсомеров — белковых комплексов, состоящих, в свою очередь, из протомеров. Нуклеиновая кислота в комплексе с белками обозначается термином нуклеокапсид. Некоторые вирусы имеют также внешнюю липидную оболочку. Размеры различных вирусов колеблются от 20 (парвовирусы) до 500 (мимивирусы) и более нанометров. Вирионы часто имеют правильную геометрическую форму (икосаэдр, цилиндр). Такая структура капсида предусматривает идентичность связей между составляющими ее белками, и, следовательно, может быть построена из стандартных белков одного или нескольких видов, что позволяет вирусу экономить место в геноме.
Процесс вирусного инфицирования
Условно процесс вирусного инфицирования в масштабах одной клетки можно разбить на несколько взаимоперекрывающихся этапов:
• проникновение в клетку
• перепрограммирование клетки
• персистенция (переход в неактивное состояние)
• создание новых вирусных компонентов
• созревание новых вирусных частиц и их выход из клетки
ПРОНИКНОВЕНИЕ В КЛЕТКУ
На этом этапе вирусу необходимо доставить внутрь клетки свою генетическую информацию. Некоторые вирусы переносят также собственные белки, необходимые для ее реализации. Различные вирусы для проникновения в клетку используют разные стратегии: например, пикорнавирусы впрыскивают свою РНК через плазматическую мембрану, а вирионы ортомиксовирусов захватываются клеткой в ходе эндоцитоза, попадают в кислую среду лизосом, где происходит их окончательное созревание (депротеинизация вирусной частицы), после чего РНК в комплексе с вирусными белками преодолевает лизосомальную мембрану и попадает в цитоплазму. Вирусы также различаются по локализации их репликации, часть вирусов (например, те же пикорнавирусы) размножается в цитоплазме клетки, а часть (например, ортомиксовирусы) — в ее ядре.
ПЕРЕПРОГРАММИРОВАНИЕ КЛЕТКИ
При заражении вирусом в клетке активируются специальные механизмы противовирусной защиты. Зараженные клетки начинают синтезировать сигнальные молекулы — интерфероны, переводящие окружающие здоровые клетки в противовирусное состояние и активирующие системы иммунитета. Повреждения, вызываемые размножением вируса в клетке, могут быть обнаружены системами внутреннего клеточного контроля, и такая клетка должна будет «покончить жизнь самоубийством» в ходе процесса, называемого апоптозом или программируемой клеточной смерти. От способности вируса преодолевать системы противовирусной защиты напрямую зависит его выживание. Неудивительно, что многие вирусы (например, пикорнавирусы, флавивирусы) в ходе эволюции приобрели способность подавлять синтез интерферонов, апоптозную программу и т.д.
Кроме подавления противовирусной защиты вирусы стремятся создать в клетке максимально благоприятные условия для развития своего потомства.
ПРИМЕР ПЕРЕПРОГРАММИРОВАНИЯ СИСТЕМ КЛЕТКИ-ХОЗЯИНА
Хрестоматийным примером перепрограммирования систем клетки-хозяина является трансляция РНК энтеровирусов (семейство пикорнавирусы). Вирусная протеаза расщепляет клеточный белок eIF4G, необходимый для инициации трансляции подавляющего большинства клеточных мРНК (транслирующихся по так называемому кэп-зависимому механизму). При этом инициация трансляции РНК самого вируса происходит другим способом (IRES-зависимый механизм), для которого вполне достаточно отрезанного фрагмента eIF4G. Таким образом, вирусные РНК приобретают эксклюзивные «права» и не конкурируют за рибосомы с клеточными.
ПЕРСИСТЕНЦИЯ
Некоторые вирусы могут переходить в латентное состояние (так называемая персистенция для вирусов эукариот или лизогения для бактериофагов — вирусов бактерий), слабо вмешиваясь в процессы, происходящие в клетке, и активироваться лишь при определенных условиях. Так построена, например, стратегия размножения некоторых бактериофагов — до тех пор, пока зараженная клетка находится в благоприятной среде, фаг не убивает ее, наследуется дочерними клетками и нередко интегрируется в клеточный геном. Однако при попадании зараженной лизогенным фагом бактерии в неблагоприятную среду возбудитель захватывает контроль над клеточными процессами, так что клетка начинает производить материалы, из которых строятся новые фаги (так называемая литическая стадия). Клетка превращается в фабрику, способную производить многие тысячи фагов. Зрелые частицы, выходя из клетки, разрывают клеточную мембрану, тем самым убивая клетку. С персистенцией вирусов (например, паповавирусов) связаны некоторые онкологические заболевания.
СОЗДАНИЕ НОВЫХ ВИРУСНЫХ КОМПОНЕНТОВ
Размножение вирусов в самом общем случае предусматривает три процесса:
Транскрипция вирусного генома, то есть синтез вирусной мРНК.
Ее трансляция, то есть синтез вирусных белков.
Репликация вирусного генома (в некоторых случаях, когда генетическая информация вируса закодирована в виде РНК, геномная РНК одновременно играет роль мРНК, и, следовательно, процесс транскрипции в паразитируемой клетке не происходит за ненадобностью).
У многих вирусов существуют системы контроля, обеспечивающие оптимальное расходование биоматериалов клетки-хозяина. Например, когда вирусной мРНК накоплено достаточно, транскрипция вирусного генома подавляется, а репликация, напротив, активируется.
СОЗРЕВАНИЕ ВИРИОНОВ И ВЫХОД ИЗ КЛЕТКИ
В конце концов новосинтезированные геномные РНК или ДНК одеваются соответствующими белками и выходят из клетки. Следует сказать, что активно размножающийся вирус не всегда убивает клетку-хозяина. В некоторых случаях (например, ортомиксовирусы) дочерние вирусы отпочковываются от плазматической мембраны, не вызывая ее разрыва. Таким образом, клетка может продолжать жить и продуцировать вирус.
Источник